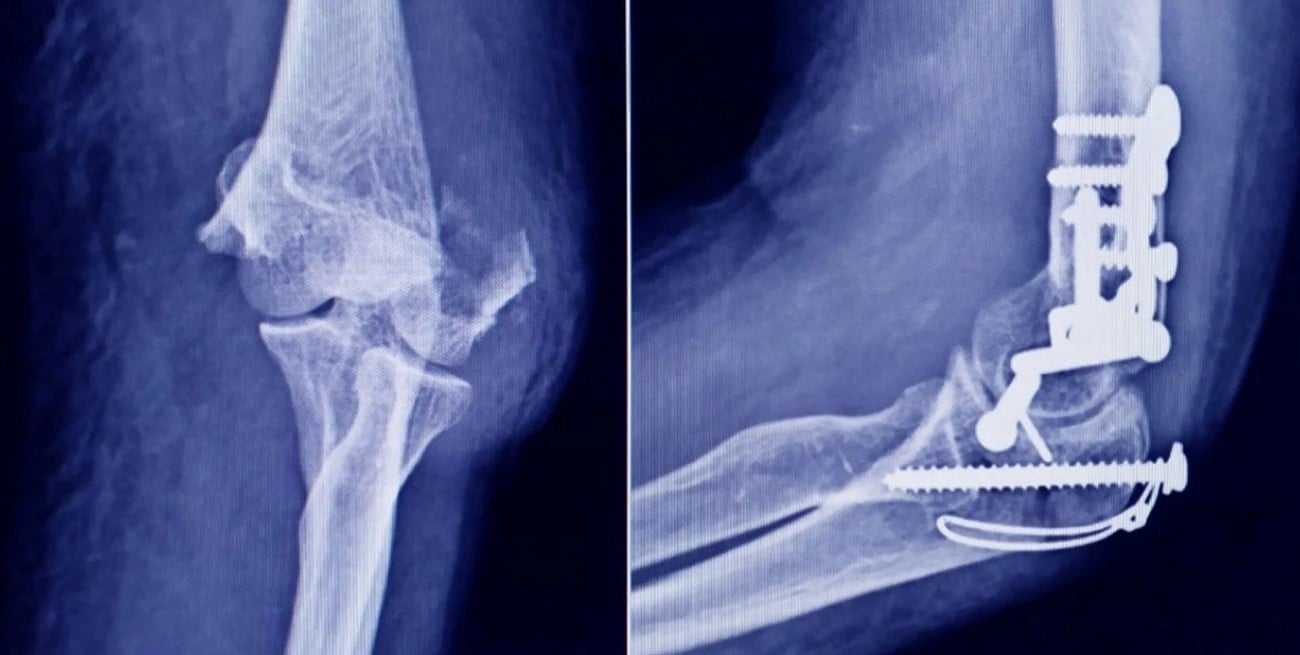
La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica dispuso la prohibición del uso, comercialización y distribución de una serie de insumos médicos utilizados en traumatología, luego de detectar graves irregularidades durante una inspección en un establecimiento de la provincia de Tucumán.
Anmat prohíbe insumos traumatológicos por falsificación y falta de control sanitario
Detectaron un tornillo quirúrgico falsificado y otros implantes sin registro legal. La medida rige en todo el país para proteger a los pacientes.
El procedimiento, realizado a fines de 2025, puso al descubierto un escenario preocupante: la presencia de un tornillo quirúrgico falsificado y otros implantes de origen desconocido, sin respaldo documental ni registro sanitario. La medida quedó formalizada en la Disposición 2223/2026, publicada en el Boletin Oficial, y tiene alcance en todo el territorio nacional.
Fallas críticas
Durante la inspección a la firma Ortopedia Tucumán de Piur SRL, los técnicos detectaron una serie de productos que no cumplían con los estándares exigidos para su uso en el sistema de salud.
El caso más relevante fue el de un tornillo de interferencia para ligamento cruzado, rotulado como perteneciente a la marca Stryker. Tras un análisis detallado, se determinó que se trataba de una falsificación.
Las diferencias con el producto original fueron contundentes. Mientras el implante legítimo presenta un color gris opaco, el detectado era incoloro y translúcido, lo que sugiere una composición distinta. Además, el empaque no coincidía con los estándares del fabricante: estaba contenido en una bolsa tipo pouch de una marca que no es utilizada por la empresa original.
Otro punto clave fue el método de esterilización. El producto auténtico se esteriliza mediante radiación gamma, mientras que el hallado indicaba haber sido preparado para esterilización por vapor o formaldehído, un procedimiento incompatible con ese tipo de dispositivo.
A esto se sumó la ausencia de datos esenciales, como la fecha de vencimiento, y la detección de que el lote correspondía a una referencia que dejó de fabricarse en 2024 y cuya vigencia original habría expirado entre 2015 y 2016.
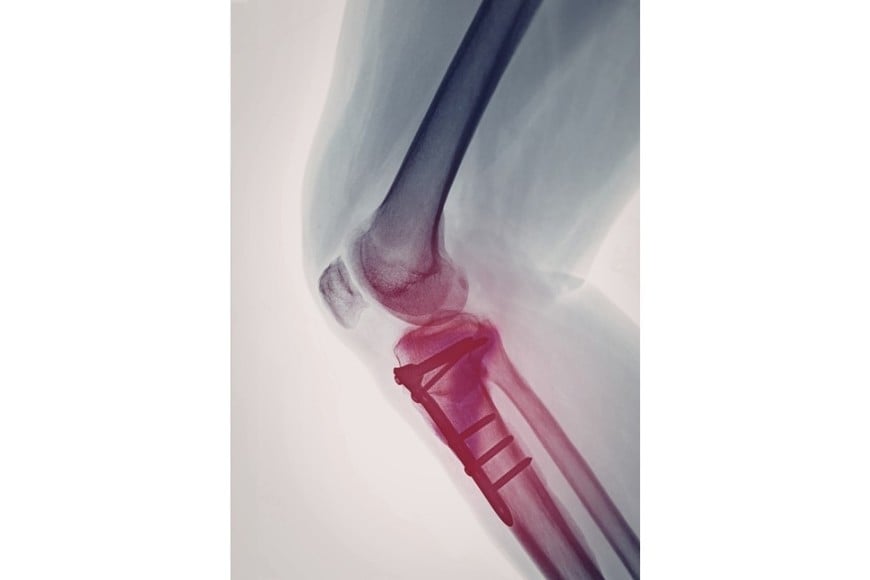
Implantes sin trazabilidad ni respaldo legal
Además del tornillo falsificado, se encontraron otros 19 implantes —tornillos óseos de titanio— rotulados como pertenecientes a fabricantes internacionales. Sin embargo, estos productos no pudieron ser validados por los importadores oficiales en Argentina.
La empresa titular del registro sanitario informó que no había ingresado esos lotes al país ni reconocía las unidades como propias. Incluso, se detectaron inconsistencias en el rotulado, que mencionaba vínculos comerciales inexistentes entre firmas internacionales.
La situación se agravó por la falta total de documentación que acreditara la procedencia de los productos. El responsable del establecimiento no pudo presentar facturas, registros de importación ni certificados sanitarios.
En términos técnicos, esto implica una ruptura completa de la trazabilidad, un elemento central en el control de dispositivos médicos. Sin esa información, resulta imposible garantizar cómo fueron fabricados, transportados o almacenados los insumos.
Riesgos para la salud
La decisión de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica se fundamenta en el potencial riesgo que estos productos representan para los pacientes.
En el caso del tornillo falsificado, la incertidumbre sobre su composición y resistencia mecánica abre la posibilidad de fallas estructurales una vez implantado. En cirugías como las de ligamento cruzado, este tipo de dispositivos cumple una función clave en la estabilidad de la articulación.
Además, el uso de métodos de esterilización inadecuados incrementa el riesgo de infecciones postquirúrgicas, una de las complicaciones más graves en este tipo de intervenciones.
Para los tornillos de titanio de origen desconocido, el riesgo radica en la falta de garantías sobre su calidad. No se puede asegurar que los materiales sean aptos para uso médico ni que cumplan con los estándares de biocompatibilidad.
También se desconoce si los productos fueron almacenados en condiciones adecuadas o si han sido retirados del mercado en otros países por fallas de funcionamiento.
Un entorno sin controles vigentes
El contexto en el que se detectaron estas irregularidades también generó preocupación. Al momento de la inspección, el establecimiento operaba con una habilitación sanitaria vencida desde marzo de 2025.
Esto implica que no contaba con supervisión estatal vigente, lo que aumenta el riesgo de que este tipo de situaciones pase inadvertido durante períodos prolongados.
Además, los productos fueron hallados en condiciones de almacenamiento poco claras, lo que refuerza la falta de control en la gestión de insumos médicos.

Medidas sanitarias y legales
Frente a este escenario, la autoridad sanitaria dispuso la prohibición total del uso, comercialización y distribución de todos los productos involucrados.
La medida tiene carácter preventivo y busca evitar que estos insumos lleguen a ser utilizados en pacientes. Al mismo tiempo, se iniciaron actuaciones administrativas para determinar las responsabilidades del establecimiento inspeccionado.
Este tipo de procedimientos puede derivar en sanciones que van desde multas hasta la clausura del local, dependiendo de la gravedad de las irregularidades detectadas.